青岛


近日,中国科学院海洋研究所张盾课题组的最新研究成果以“"Nano Killers" Activation by Permonosulfate Enables Efficient Anaerobic Microorganisms Disinfection”为题发表在Journal of hazardous materials。
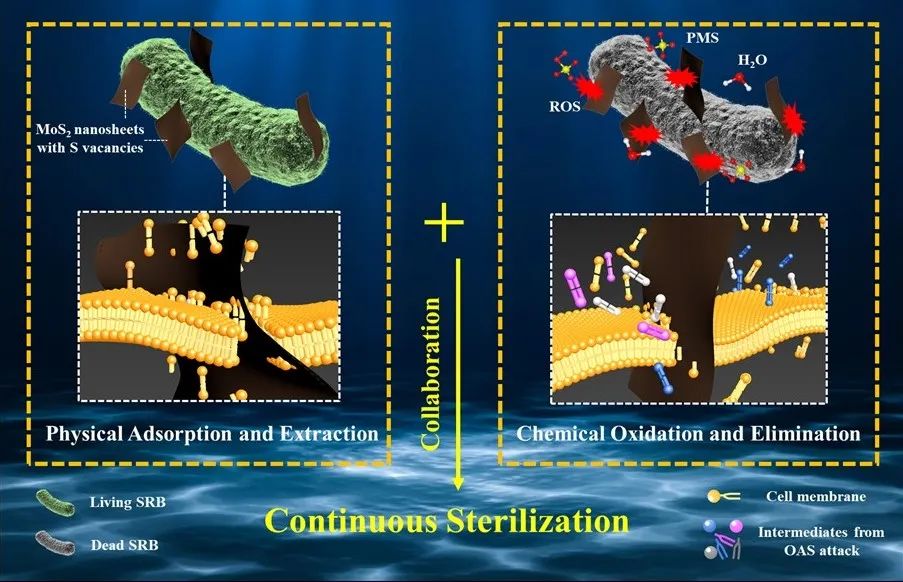
研究基于MoS2(二硫化钼)纳米片物理损伤和化学氧化的协同作用,构建了一种快速高效的针对厌氧细菌的杀菌体系。MoS2纳米片的“刀片状”边缘可以插入细胞膜并提取脂质。由于Mo(钼)的高效电子转移能力和MoS2中的S(硫)空位对过硫酸盐和水的强吸附作用,MoS2可催化产生SO4·-和·OH。这些物质会攻击MoS2表面的脂质,实现杀菌。通过物理损伤和化学消除的协同作用,可以实现在各种环境中的快速稳定的灭菌工作。这项工作将为拓展厌氧杀菌机制提供重要参考价值。
海洋环境中的微生物污损和微生物引起的腐蚀是严重的经济和安全问题,我国腐蚀造成的经济损失约占当年GDP的3.34%,而海洋腐蚀损失约占总腐蚀损失的1/3,超过7000亿元,随着海洋环境恶化,经济损失可能会增加。在腐蚀细菌中,广泛分布于缺氧环境中的硫酸盐还原菌(Sulfate-Reducing Bacteria,SRB)长期以来一直被普遍认为是导致金属材料腐蚀失效的罪魁祸首。近期,具有细胞毒性的材料引起了广泛关注。MoS2纳米片是典型的二维材料,由于S和脂质之间的静电效应和范德华力,表现出显著的细胞毒性,MoS2中的负硫很容易与脂质的亲水性头部结合,从而MoS2的边缘可以像“刀”一样切开细胞膜,提取脂质,最终导致细胞死亡。研究表明,MoS2中的S空位对过硫酸盐(permonosulfate, PMS)和水具有强吸附作用,可催化二者产生强氧化性自由基。因此,利用MoS2的这两个特性,可以提出针对厌氧微生物的新的杀菌机制。
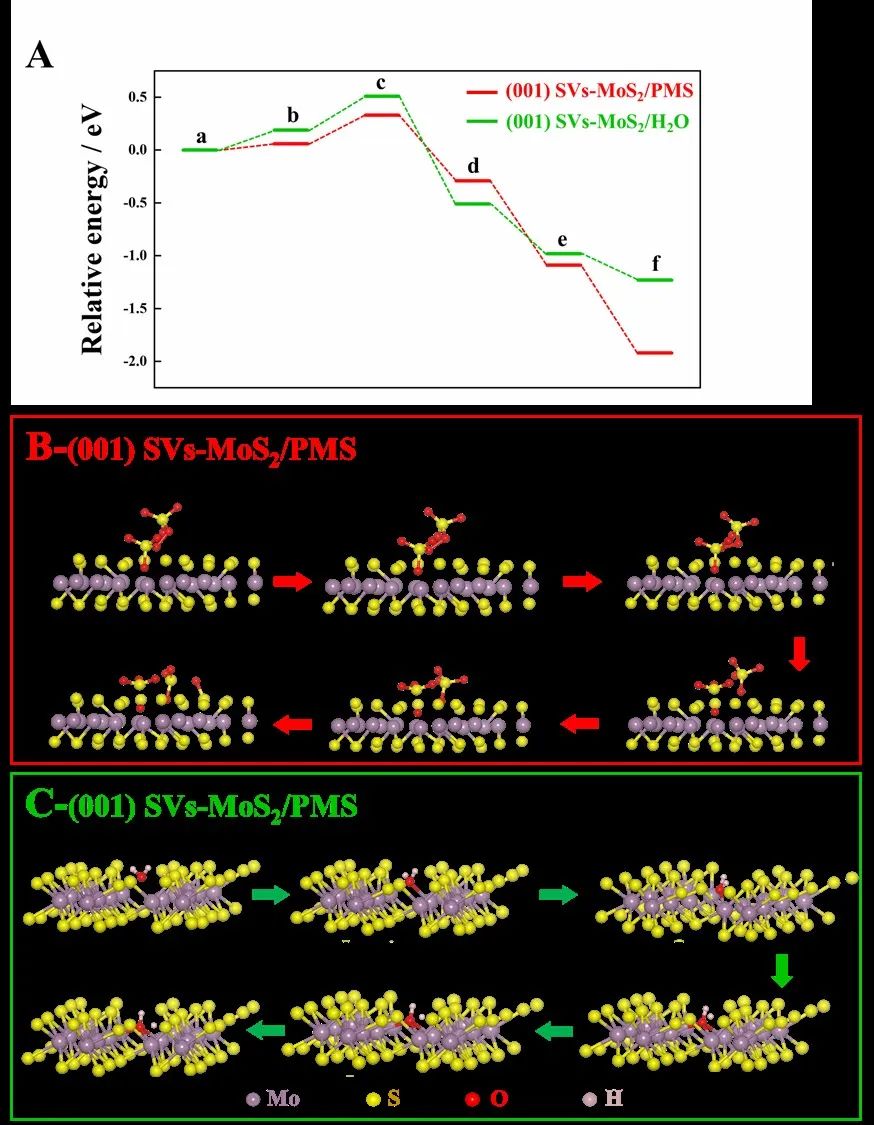
研究通过MoS2的物理和化学协同作用杀灭厌氧微生物,如图1所示,针对SRB和PA,在PMS的辅助下,添加低浓度MoS2就可以实现高效杀菌率,如图2,杀菌机理如图3所示。根据第一性原理计算分析,相较于H2O,MoS2吸附PMS具有更低的能垒,因此,PMS在MoS2表面比H2O更容易被吸收和激发。MoS2吸附H2O和PMS后,经过一系列中间体的变化,生成强氧化性自由基,这些自由基会攻击细菌细胞膜上的脂质,最终导致细菌的死亡。
图1 物理提取和化学氧化协同的厌氧杀菌机制示意图
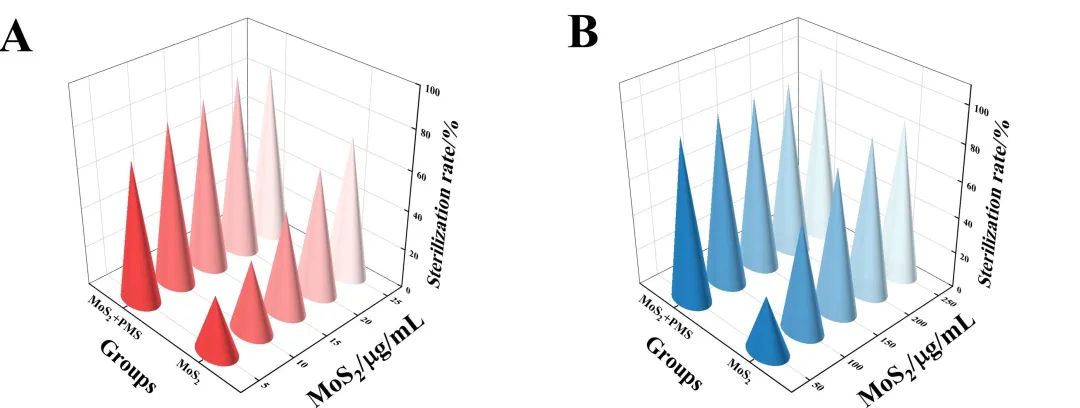
图2 不同处理下,针对(A)SRB和(B)PA的杀菌率
图3(A)催化过程中涉及的过渡态的相对能量值(B)MoS2中的(001)晶面催化PMS的关键中间体和过渡态的结构(C)MoS2中的(001)晶面催化H2O的关键中间体和过渡态的结构
论文第一作者为中国科学院海洋研究所博士后王瑾,通讯作者为王毅研究员和张盾研究员。研究得到了国家自然科学基金(41976032和42176047)、“科学”高端用户项目(KEXUE2019GZ01)和2018年山东省海洋科技项目的支持。
本文来源:中国科学院海洋研究所